
北京海岸鴻蒙標(biāo)準(zhǔn)物質(zhì)技術(shù)有限責(zé)任公司
 白金會員
白金會員 已認(rèn)證
已認(rèn)證


北京海岸鴻蒙標(biāo)準(zhǔn)物質(zhì)技術(shù)有限責(zé)任公司
 白金會員
白金會員 已認(rèn)證
已認(rèn)證

近年來,隨著醫(yī)療健康行業(yè)的快速發(fā)展,藥品質(zhì)量安全問題引起了社會的廣泛關(guān)注。
一、2024年數(shù)據(jù)統(tǒng)計1、2024年5月22日,浙江省藥品監(jiān)督管理局發(fā)布2024年第1期浙江省藥品質(zhì)量抽查檢驗公告的通知:浙江省藥品監(jiān)督管理局組織開展了對轄區(qū)內(nèi)藥品生產(chǎn)、經(jīng)營和使用單位的相關(guān)藥品質(zhì)量監(jiān)督抽檢,標(biāo)示為上海某某金朱藥業(yè)生產(chǎn)的1批次利巴韋林注射液和上海某某林州制藥有限公司生產(chǎn)的1批次維生素 B12注射液不符合規(guī)定,不符合規(guī)定項目為【檢查】可見異物。省藥品監(jiān)督管理局已要求各相關(guān)地市市場監(jiān)督管理部門依法處置。
2、2024年5月29日,安徽省藥品監(jiān)督管理局發(fā)布2024第5期藥品質(zhì)量公告:經(jīng)安徽省宿州市食品藥品檢驗檢測中心檢驗,標(biāo)示為浙江某某藥業(yè)股份有限公司生產(chǎn)的1批次氯化鈉注射液不符合規(guī)定,不符合規(guī)定項目為【檢查】可見異物。
3、2024年8月5日,上海市藥品監(jiān)督管理局發(fā)布關(guān)于2024年第1期藥品質(zhì)量抽檢通告:上海市藥品監(jiān)督管理局組織相關(guān)單位對本市藥品生產(chǎn)、經(jīng)營和使用單位開展了藥品質(zhì)量抽檢,標(biāo)示為某某健康管理股份有限公司生產(chǎn)的1批次氯化鈉注射液不符合規(guī)定,不符合規(guī)定項目為【檢查】可見異物。藥品監(jiān)管部門已要求相關(guān)企業(yè)采取停售、停用、召回等風(fēng)險控制措施,并對相關(guān)企業(yè)依法查處。

4、2024年11月26日,國家藥監(jiān)局發(fā)布關(guān)于28批次藥品不符合規(guī)定的通告(2024年第51號),經(jīng)安徽省食品藥品檢驗研究院檢驗,標(biāo)示為石家莊某某藥業(yè)有限公司、江蘇某某藥業(yè)有限公司、廣東某某制藥有限公司生產(chǎn)的8批次阿昔洛韋滴眼液不符合規(guī)定,不符合規(guī)定項目為可見異物。對上述不符合規(guī)定藥品,藥品監(jiān)督管理部門已要求相關(guān)企業(yè)和單位采取暫停銷售使用、召回等風(fēng)險控制措施,對不符合規(guī)定原因開展調(diào)查并切實進行整改。同時,國家藥品監(jiān)督管理局要求相關(guān)省級藥品監(jiān)督管理部門依據(jù)《中華人民共和國藥品管理法》,組織對上述企業(yè)和單位存在的涉嫌違法行為立案調(diào)查,并按規(guī)定公開查處結(jié)果。
二、藥品中可見異物問題近5年趨勢
我們看一組數(shù)據(jù)對比,隨著2019年修訂的《中華人民共和國藥品管理法》全面貫徹落實了“四個最嚴(yán)”要求,即最嚴(yán)謹(jǐn)?shù)臉?biāo)準(zhǔn)、最嚴(yán)格的監(jiān)管、最嚴(yán)厲的處罰和最嚴(yán)肅的問責(zé),以及《中國藥典》2020年版對可見異物檢測的明確規(guī)定,2020年之后,關(guān)于藥品中可見異物的改善已經(jīng)有了顯著的進展,被公告的企業(yè)大幅減少。
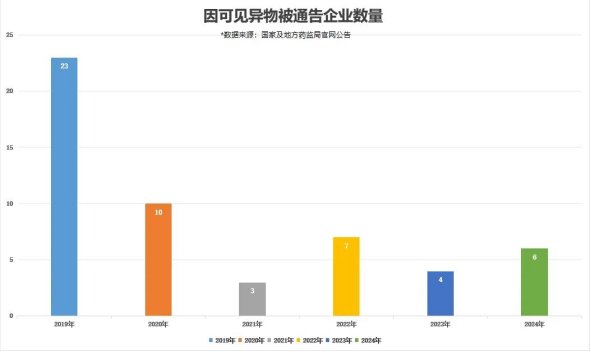
由此可見,藥品中的可見異物問題是可控的!在藥企和藥品監(jiān)管部門等相關(guān)機構(gòu)的共同努力下,藥品中的可見異物或?qū)⒉辉僖姡?/span>
在注射劑企業(yè)中,通常使用有證可見異物標(biāo)準(zhǔn)物質(zhì)或自行制備缺陷品進行質(zhì)量控制。但從準(zhǔn)確性角度看,有證可見異物標(biāo)準(zhǔn)物質(zhì)經(jīng)過嚴(yán)格的測試和驗證,它們的特性明確,能夠有效幫助檢測人員在實際操作中快速識別異物的類型和特征;從合規(guī)性角度看,有證可見異物標(biāo)準(zhǔn)物質(zhì)是經(jīng)國家市場監(jiān)督總局批準(zhǔn)的國家標(biāo)準(zhǔn)物質(zhì),該產(chǎn)品是用標(biāo)稱粒徑的單分散聚苯乙烯乳膠微粒,配制成所需濃度的微粒懸浮液。符合《中國藥典2020版:0904可見異物檢查法》的技術(shù)要求,采用顯微鏡結(jié)合圖像分析法進行定值,結(jié)果可溯源至國家長度基準(zhǔn)。
有證可見異物標(biāo)準(zhǔn)物質(zhì)在儀器檢定、儀器質(zhì)量控制、人員培訓(xùn)等領(lǐng)域的應(yīng)用,使檢測結(jié)果具備溯源性,不但保證了儀器的可用性,還可評估儀器的適用性,保證了人員目視的準(zhǔn)確性,是檢查過程中必備的一環(huán)。
三、如何選用合適的可見異物標(biāo)準(zhǔn)物質(zhì)?
1、首先,看證書。不是所有廠家生產(chǎn)的可見異物標(biāo)準(zhǔn)物質(zhì)都有國家標(biāo)準(zhǔn)物質(zhì)定級證書的,目前國內(nèi)唯一一張證書在北京海岸鴻蒙標(biāo)準(zhǔn)物質(zhì)技術(shù)有限責(zé)任公司。


2、可見異物的檢查方法有人工燈檢法和光散射法兩大類。人工燈檢法是各國藥典均采用的檢查方法,光散射法是ChP 0904可見異物檢查法中的第二法,USP<1790>中還介紹了半自動燈檢法和全自動燈檢機法。兩種檢查方法配套的產(chǎn)品有所區(qū)別。
2-1 人工燈檢法用可見異物標(biāo)準(zhǔn)物質(zhì)
常規(guī)包裝為2mL/ 5mL/10mL安瓿瓶或西林瓶。為注射液、眼用液體制劑或其他藥液中可見異物檢查專用標(biāo)準(zhǔn)物質(zhì)。可用于形式評價和檢驗分析方法,檢測人員培訓(xùn)和考核。
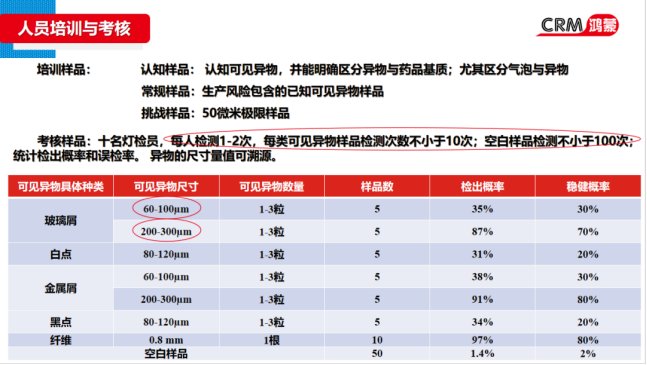
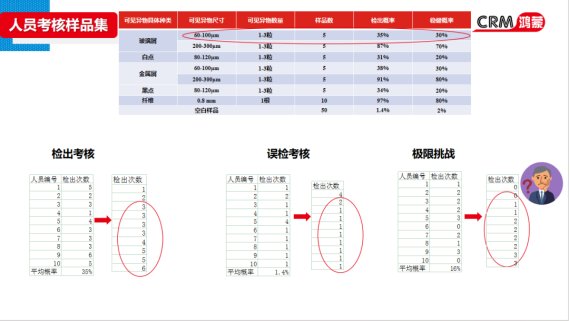
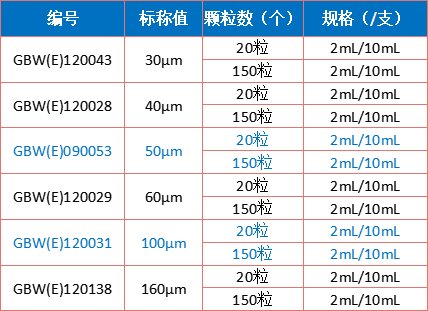
2-2 全自動燈檢機用可見異物標(biāo)準(zhǔn)物質(zhì)

符合《JJF1824-2020 全自動燈檢機校準(zhǔn)規(guī)范》

全自動燈檢機校準(zhǔn)用標(biāo)準(zhǔn)物質(zhì)用標(biāo)稱粒徑的單分散聚苯乙烯乳膠微粒,配制成所需濃度的微粒懸浮液,包括4種微粒標(biāo)準(zhǔn)物質(zhì)。完全滿足JJF 1824-2020《全自動燈檢機校準(zhǔn)規(guī)范》的技術(shù)要求。采用顯微鏡結(jié)合圖像分析法對顆粒粒徑進行定值,定值結(jié)果可溯源至國家長度基準(zhǔn)。
本標(biāo)準(zhǔn)物質(zhì)為250瓶/套,其中80支微粒標(biāo)準(zhǔn)物質(zhì),170支空白液,可根據(jù)用戶需求制成不同規(guī)格與包裝。
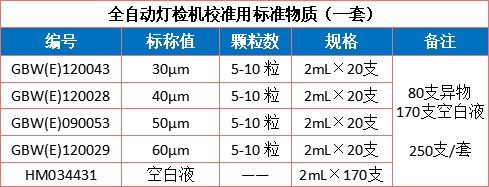
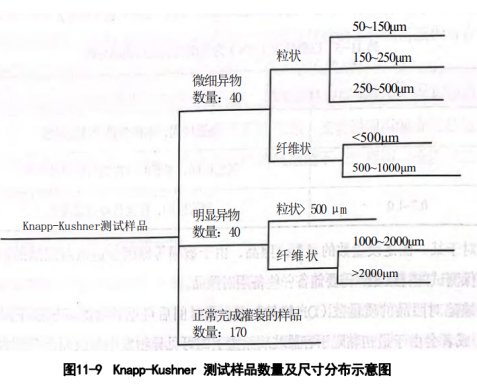
3、GMP無菌制劑——Knapp 測試樣品要求及配套方案:
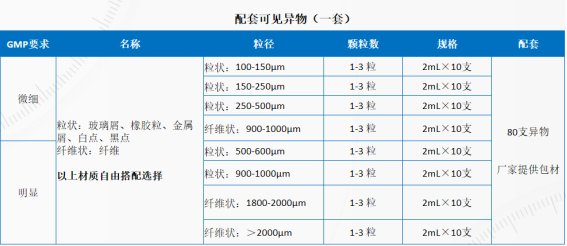
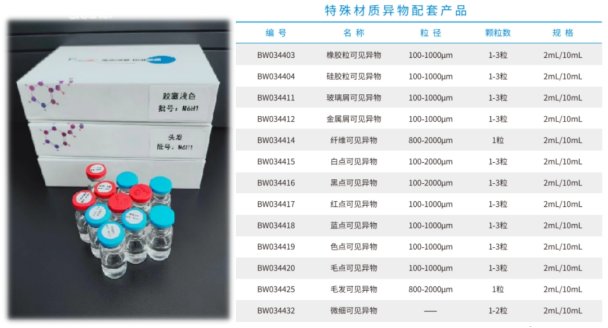
4、可定制特殊材質(zhì)可見異物
最新動態(tài)
更多




虛擬號將在 秒后失效
使用微信掃碼撥號